Širdies nepakankamumas su sumažėjusia išstūmimo frakcija (HFrEF) yra pagrindinė širdies nepakankamumo rūšis, o Kinijos HF tyrimas parodė, kad 42% širdies nepakankamumo atvejų Kinijoje yra HFrEF, nors yra keletas standartinių terapinių vaistų, skirtų HFrEF gydyti, ir sumažino riziką. mirties ir hospitalizavimo dėl širdies nepakankamumo tam tikru mastu. Tačiau pacientams yra didelė pasikartojančių širdies nepakankamumo pasunkėjimo reiškinių rizika, mirštamumas išlieka apie 25%, o prognozė tebėra prasta. Todėl vis dar skubiai reikia naujų terapinių agentų gydant HFrEF, o Vericiguat, naujas tirpus guanilato ciklazės (sGC) stimuliatorius, buvo tiriamas VICTORIA tyrime, siekiant įvertinti, ar Vericiguat gali pagerinti pacientų, sergančių HFrEF, prognozę. Tyrimas yra daugiacentris, atsitiktinių imčių, lygiagrečių grupių, placebu kontroliuojamas, dvigubai aklas, įvykiais pagrįstas III fazės klinikinių rezultatų tyrimas. Tyrime, kurį globoja VIGOR centras Kanadoje, bendradarbiaujant su Duke klinikinių tyrimų institutu, dalyvavo 616 centrų 42 šalyse ir regionuose, įskaitant Europą, Japoniją, Kiniją ir JAV. Mūsų kardiologijos skyriui buvo didelė garbė dalyvauti. Iš viso 5050 pacientų, sergančių lėtiniu širdies nepakankamumu, ≥18 metų amžiaus, NYHA II-IV klasės, EF <45%, kurių natriurezinio peptido (NT-proBNP) kiekis buvo padidėjęs per 30 dienų iki atsitiktinės atrankos ir kurie buvo hospitalizuoti dėl širdies nepakankamumo. į tyrimą buvo įtraukti per 6 mėnesius iki atsitiktinės atrankos arba per 3 mėnesius iki atsitiktinės atrankos buvo į veną sušvirkšti diuretikų širdies nepakankamumui gydyti, visi, gaunantys ESC, AHA/ACC ir nacionalines/regionines rekomendacijas, rekomenduojamą priežiūros standartą. Pacientai buvo atsitiktinai suskirstyti į dvi grupes santykiu 1:1 ir jiems buvo suteiktaVericiguat(n=2526) ir placebas (n=2524) kartu su standartine terapija.
Pirminė tyrimo baigtis buvo sudėtinė baigtis – mirtis dėl širdies ir kraujagyslių ligų arba pirmasis hospitalizavimas dėl širdies nepakankamumo; antrinės vertinamosios baigtys apėmė pirminės vertinamosios baigties komponentus, pirmąjį ir vėlesnį širdies nepakankamumo hospitalizavimą (pirmuosius ir pasikartojančius įvykius), sudėtinį baigtį – mirtį dėl bet kokios priežasties arba hospitalizavimą dėl širdies nepakankamumo ir mirtį dėl bet kokios priežasties. Vidutiniškai 10,8 mėnesio stebėjimo laikotarpiu, Vericiguat grupėje, palyginti su placebo grupe, pirminė vertinamoji baigtis – mirtis dėl širdies ir kraujagyslių ligų arba pirmasis hospitalizavimas dėl širdies nepakankamumo – sumažėjo santykinai 10 %.
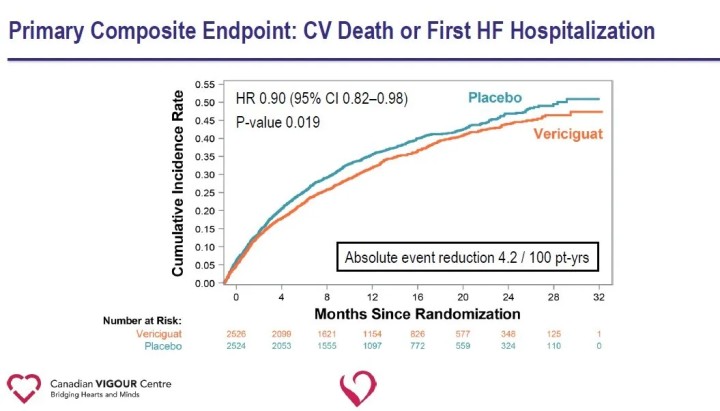
Antrinių vertinamųjų baigčių analizė parodė, kad Vericiguat grupėje, palyginti su placebo grupe, reikšmingai sumažėjo hospitalizavimo dėl širdies nepakankamumo atvejų (HR 0,90) ir reikšmingai sumažėjo sudėtinis mirtingumas arba hospitalizavimas dėl širdies nepakankamumo (HR 0,90).
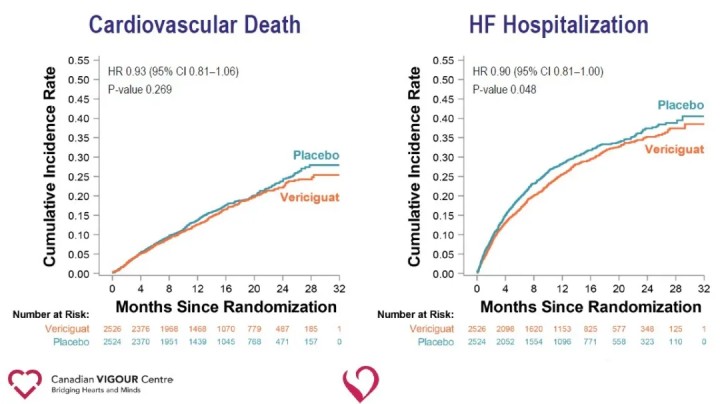
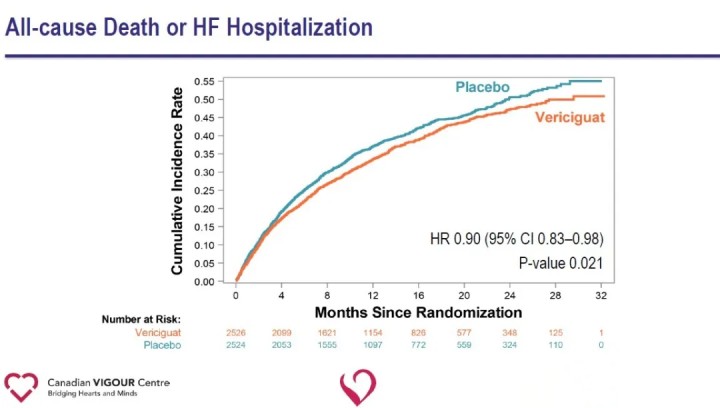
Tyrimo rezultatai rodo, kad pridėjusVericiguatStandartinis širdies nepakankamumo gydymas žymiai sumažina pastaruoju metu pablogėjusių širdies nepakankamumo reiškinių dažnį ir sumažina sudėtinio kardiovaskulinės mirties arba hospitalizavimo dėl širdies nepakankamumo riziką pacientams, sergantiems HFrEF. Vericiguat gebėjimas sumažinti sudėtinio mirties nuo širdies ir kraujagyslių ligų ar širdies nepakankamumo hospitalizavimo riziką pacientams, sergantiems didelės rizikos širdies nepakankamumu, suteikia naują širdies nepakankamumo gydymo būdą ir atveria naujus būdus ateityje tirti širdies ir kraujagyslių ligas. Vericiguat šiuo metu nepatvirtintas prekybai. Vaisto saugumas, veiksmingumas ir ekonomiškumas dar turi būti toliau tikrinami rinkoje.
Paskelbimo laikas: 2022-09-09
